Киселинско-базната рамнотежа. На регулирање на концентрацијата на водородни јони
Видео: Киселина-база титрација - Метод за определување на концентрацијата на киселина или база во раствор
Cодржина
механизми за регулација содржината на водородни јони (H +) во телото во многу начини слични на одржување на балансот на други јони. На пример, за да се постигне хомеостаза потребно кореспонденција помеѓу доаѓањето (форма) од H + јони и да ги изолираат од организми mA. Бубрезите да игра водечка улога во отстранувањето на јони од телото Хм. Прецизно регулирање на содржината на H + во екстрацелуларната течност не е само распредели нивната бубрезите. Покрај тоа, во телото голем број на повеќе механизми како пуфер со што концентрацијата на H + јони во течност медиуми се одржува во нормална urovne- тие ги вклучуваат крвниот систем, респираторниот систем и процесите кои се случуваат на ниво на клетка.
Видео: Киселина база титрација
Оваа статија се дискутира улогата на различните фактори, кои придонесуваат за одржување на одредена концентрација од H + јони. Во оваа специјална улога на реапсорпција и секреција на H + јоните во тубулите, како и формирање и екскреција на бикарбонат (HCO 3) од страна на бубрезите, бидејќи овие супстанции главно се одреди статусот на ацидо-базната рамнотежа во течни медиуми.
точниот Регулирање на содржината од H + јони Тоа е од големо значење, бидејќи концентрацијата на јоните влијае на активноста на речиси сите системи на ензими во телото. Во врска со оваа промена во нивната содржина влијае речиси секоја клетка и телото функции.
Видео: Решение на "соли хидролиза" №7

Во споредба со другите јони H + јон концентрација во течни медиуми обично се одржува на ниско ниво. На пример, концентрацијата на натриум во екстрацелуларната течност (142 mEq / l) е скоро 3,5 милиони пати повисока од содржината на H + јони за кои просеци ,00004 mEq / L. Нормалата за H + јоните е исто така дел од опсегот 1/106 јонски осцилации Na +, така да се одржи на бројни клеточни функции неопходни за регулирање на содржината на H + јоните со висока точност.
H честички (Proton) е дел од молекулот на водород. Молекули кои може да одвои за да се формира H + јоните, наречен киселини. Еден пример на ова соединение - хлороводородна киселина (HCl), која се одделува во водата во водород јони (H +) и хлорид јон (Cl-). Таквите дисоцијација се случува во молекула и јаглеродна киселина (H2CO3), што резултира во формирање на H + јон и бикарбонат (NPHS).
Основите наведени јони или молекули, се способни за врзување со протон. База, на пример, може да се смета HCO3, бидејќи бикарбонат јон е во состојба да се обединат со H + јони да формираат H2CO3. Бикарбонатни јони како фосфат (HPO4) како што се основа на: прикачување на протонска, тие формираат N2R04. На протеините во организмот, исто така, функционира како база носат негативен полнеж и лесно да се поврзе H + јони. Најважните од нив се на хемоглобинот од црвените крвни зрнца и интрацелуларни протеини.
Термините "основи"И"бази"Често се користат наизменично. На алкално е молекул, кој вклучува еден или повеќе алкални метали - натриум, калиум, литиум, итн, и силна база, како што се, на пример, хидроксил јон (OH-) .. Некои од овие молекули претставен од страна на база реагира брзо со H + јони во раствор поврзувајќи ги, па алкална се однесуваат на типичен причини. Недостаток на протоните во течни медиуми од алкалоза, а вишокот - ацидоза.
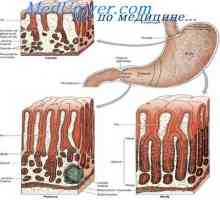 Физиологија на плунка. лачење плунка
Физиологија на плунка. лачење плунка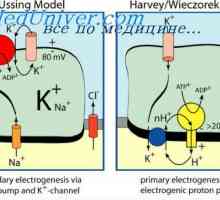 Kontrtransport калциум и водородни јони. Активен транспорт до ткивата
Kontrtransport калциум и водородни јони. Активен транспорт до ткивата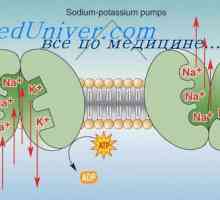 Улогата на Na-K-пумпа. Активен транспорт на јони на калциум и водород во клетката
Улогата на Na-K-пумпа. Активен транспорт на јони на калциум и водород во клетката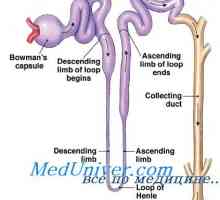 Секреција на калиум примарен бубрежни клетки. Фактори регулирање на секреција на калиум
Секреција на калиум примарен бубрежни клетки. Фактори регулирање на секреција на калиум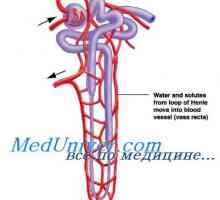 Влијанието на ацидоза на калиум размена. Механизми за регулирање на концентрација на калциум
Влијанието на ацидоза на калиум размена. Механизми за регулирање на концентрација на калциум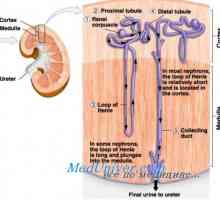 Ефект на алдостеронот на калиум размена. Зависност калиум секреција на алдостерон
Ефект на алдостеронот на калиум размена. Зависност калиум секреција на алдостерон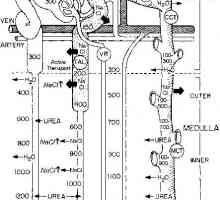 Учество во бубрезите магнезиум размена. Прилагодување на јачината на звукот на интерстицијална…
Учество во бубрезите магнезиум размена. Прилагодување на јачината на звукот на интерстицијална…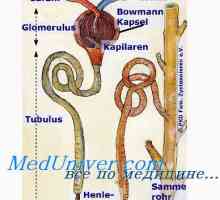 Одржување на концентрацијата на водородни јони. Функцијата на тампон системи
Одржување на концентрацијата на водородни јони. Функцијата на тампон системи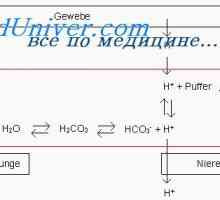 Хендерсон-Hasselbach равенка. тампон резервоар
Хендерсон-Hasselbach равенка. тампон резервоар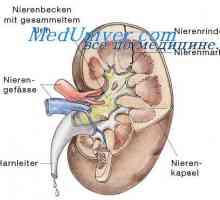 Силни и слаби киселини и бази. Концентрацијата на водородни јони и pH
Силни и слаби киселини и бази. Концентрацијата на водородни јони и pH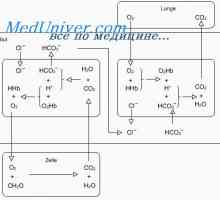 Бикарбонат пуфер систем. Системот на фосфатен пуфер
Бикарбонат пуфер систем. Системот на фосфатен пуфер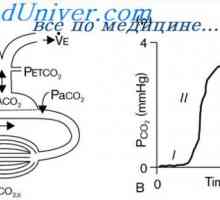 На капацитет на пуфер на респираторниот систем. Учество на бубрежната регулирање на…
На капацитет на пуфер на респираторниот систем. Учество на бубрежната регулирање на…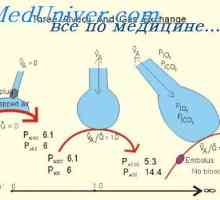 Влијанието на алвеоларна вентилација на pH вредност. Ефект на pH на респираторниот систем
Влијанието на алвеоларна вентилација на pH вредност. Ефект на pH на респираторниот систем Неутрализација бубрезите протони. Примарен механизам на секреција на активните водородни јони…
Неутрализација бубрезите протони. Примарен механизам на секреција на активните водородни јони…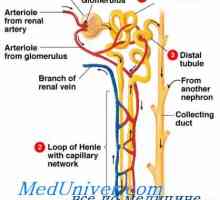 Зависноста на секреција од страна на протоните на бубрезите. Механизми на протонска секреција во…
Зависноста на секреција од страна на протоните на бубрезите. Механизми на протонска секреција во…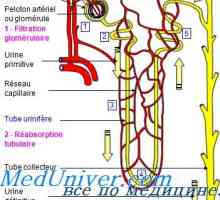 Корекција на Алкалозата бубрезите. Механизмите на ренална корекција на алкалоза
Корекција на Алкалозата бубрезите. Механизмите на ренална корекција на алкалоза Механизмот на формирање на нови бикарбонатни јони. Фосфатен пуфер бубрежна систем
Механизмот на формирање на нови бикарбонатни јони. Фосфатен пуфер бубрежна систем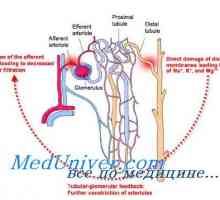 Корекција на ацидоза на бубрезите. Механизми за корекција бубрежна ацидоза
Корекција на ацидоза на бубрезите. Механизми за корекција бубрежна ацидоза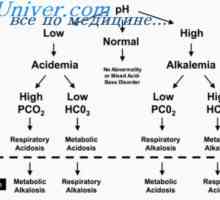 Амониум пуфер систем. Квантификација на киселини и бази распределба
Амониум пуфер систем. Квантификација на киселини и бази распределба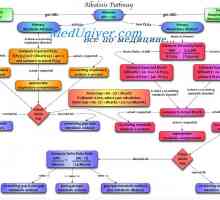 Причините за метаболна алкалоза. Третман на ацидоза и алкалоза
Причините за метаболна алкалоза. Третман на ацидоза и алкалоза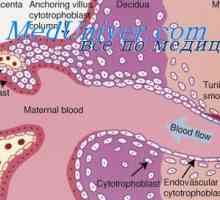 На активност на респираторниот центар. Хемиски регулирање на дишењето
На активност на респираторниот центар. Хемиски регулирање на дишењето
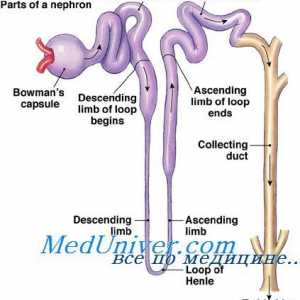 Секреција на калиум примарен бубрежни клетки. Фактори регулирање на секреција на калиум
Секреција на калиум примарен бубрежни клетки. Фактори регулирање на секреција на калиум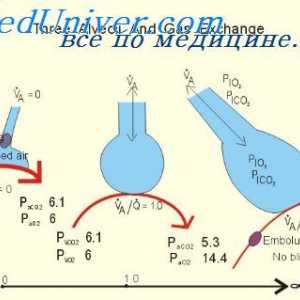 Влијанието на алвеоларна вентилација на pH вредност. Ефект на pH на респираторниот систем
Влијанието на алвеоларна вентилација на pH вредност. Ефект на pH на респираторниот систем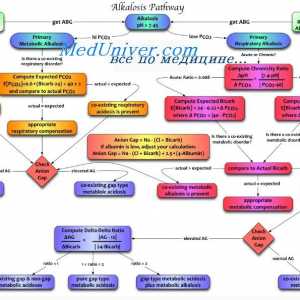 Причините за метаболна алкалоза. Третман на ацидоза и алкалоза
Причините за метаболна алкалоза. Третман на ацидоза и алкалоза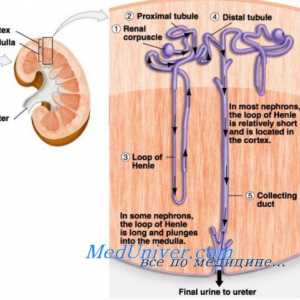 Ефект на алдостеронот на калиум размена. Зависност калиум секреција на алдостерон
Ефект на алдостеронот на калиум размена. Зависност калиум секреција на алдостерон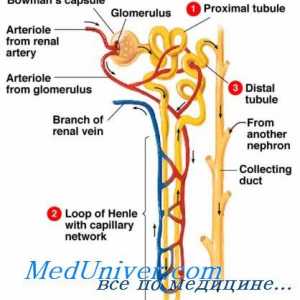 Зависноста на секреција од страна на протоните на бубрезите. Механизми на протонска секреција во…
Зависноста на секреција од страна на протоните на бубрезите. Механизми на протонска секреција во…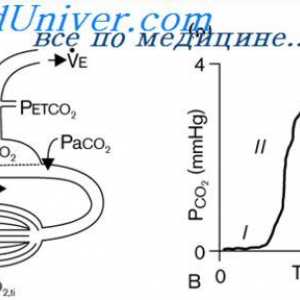 На капацитет на пуфер на респираторниот систем. Учество на бубрежната регулирање на…
На капацитет на пуфер на респираторниот систем. Учество на бубрежната регулирање на…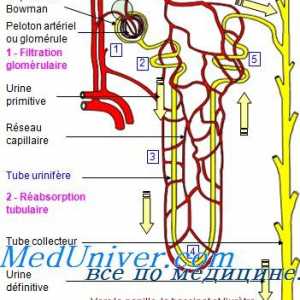 Корекција на Алкалозата бубрезите. Механизмите на ренална корекција на алкалоза
Корекција на Алкалозата бубрезите. Механизмите на ренална корекција на алкалоза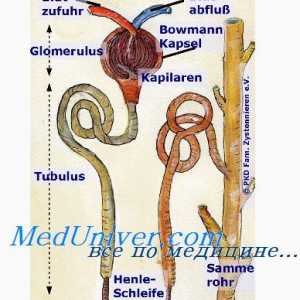 Одржување на концентрацијата на водородни јони. Функцијата на тампон системи
Одржување на концентрацијата на водородни јони. Функцијата на тампон системи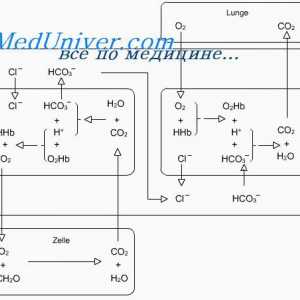 Бикарбонат пуфер систем. Системот на фосфатен пуфер
Бикарбонат пуфер систем. Системот на фосфатен пуфер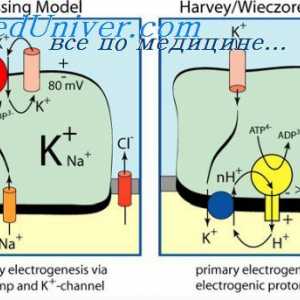 Kontrtransport калциум и водородни јони. Активен транспорт до ткивата
Kontrtransport калциум и водородни јони. Активен транспорт до ткивата